Psoriasis
Epidemiologische und klinische Studien haben durchweg gezeigt, dass Psoriasis mit einem erhöhten kardiovaskulären Risiko verbunden ist. Die in psoriatischen Läsionen gefundenen entzündlichen Zytokine können eine Insulinresistenz verursachen und eine Dysfunktion der Endothelzellen auslösen, die zu Atherosklerose und schließlich zu einem Schlaganfall oder Herzinfarkt führt[4]. Zwingende Beweise deuten außerdem darauf hin, dass pro-inflammatorische Zytokine wie Interleukin (IL)-1, IL-6 und Tumor-Nekrose-Faktor (TNF)-α die Funktion von Hepatozyten und arteriellen glatten Muskelzellen verändern können, um eine veränderte Lipoproteinzusammensetzung zu induzieren, die Expression zellulärer Adhäsionsmoleküle zu steigern und die Lipidablagerung an den Arterienwänden zu erhöhen. All diese Faktoren können zur Entstehung von Arterienplaques beitragen. Zytokine können dann die Plaque destabilisieren, indem sie die Ruptur fragiler Neo-Gefäße fördern und die Expression der fibrösen Kappe der Plaque erhöhen. Diese Kaskade von Ereignissen kann schließlich zur Plaqueruptur und zur Bildung von lebensbedrohlichen Thromben führen.
Die Psoriasis steht in signifikantem Zusammenhang mit einer höheren Prävalenz und Inzidenz von Dyslipidämie[5] – einem bekannten Risikofaktor für Herz-Kreislauf-Erkrankungen. Dyslipidämie ist ein weit gefasster Begriff, der alle Anomalien der Plasmalipide beschreibt, einschließlich Störungen des Plasmalipidspiegels oder Anomalien der Lipidzusammensetzung. Mehrere Messgrößen der Dyslipidämie sind signifikant betroffen und umfassen erhöhte Triglyzeride, erhöhtes LDL-Cholesterin, erniedrigtes HDL-Cholesterin, erhöhtes Cholesterin und erhöhte Lipoproteine [[6]].
Bei der Entwicklung von Psoriasis spielen auch die Lebensführung (Rauchen, Alkohol, BMI (Body Mass Index) Bluthochdruck, Diabetes aber auch die psychische Verfassung eine Rolle[7]. Dies wiederum spiegelt sich im Mikrobiom wider.
[1] Kurd SK, Gelfand JM. The prevalence of previously diagnosed and undiagnosed psoriasis in US adults: results from NHANES 2003-2004. J Am Acad Dermatol. 2009; 60:218–24.
[2] Menter A, Gelfand JM, Connor C, et al. Joint American Academy of Dermatology-National Psoriasis Foundation guidelines of care for the management of psoriasis with systemic nonbiologic therapies. J Am Acad Dermatol. 2020; 82:1445–86.
[3] Yang Q, Qu L, Tian H, et al. Prevalence and characteristics of psoriatic arthritis in Chinese patients with psoriasis. J Eur Acad Dermatol Venereol. 2011; 25:1409–14.
[4] Boehncke WH, Boehncke S, Tobin AM, et al. The ‘psoriatic march’: a concept of how severe psoriasis may drive cardiovascular comorbidity. Exp Dermatol. 2011; 20:303–7.
[5] Ma C, Harskamp CT, Armstrong EJ, et al. The association between psoriasis and dyslipidaemia: a systematic review. Br J Dermatol. 2013; 168:486–95.
[6] Tekin NS, Tekin IO, Barut F, et al. Accumulation of oxidized low-density lipoprotein in psoriatic skin and changes of plasma lipid levels in psoriatic patients. Mediat Inflamm. 2007; 2007:78454.
[7] The difference of lipid profiles between psoriasis with arthritis and psoriasis without arthritis and sexspecific downregulation of methotrexate on the apolipoprotein B/apolipoprotein A-1ratio. Bing Wang1†, Hui Deng2†, Yao Hu3†, Ling Han1, Qiong Huang1, Xu Fang1, Ke Yang4, Siyuan Wu1, Zhizhong Zheng1, Nikhil Yawalkar5, Zhenghua Zhang1* and Kexiang Yan1*. Wang et al. Arthritis Research & Therapy (2022) 24:17
Das Mikrobiom spielt eine wesentliche Rolle bei der Modulation des Immunsystems
Das Mikrobiom des Menschen besteht aus Bakterien (Einzellern) und Pilzen (das sind meist kleinere Zellverbände). Es umfasst nach heutigen Schätzungen etwa 39 Billionen dieser Mikroorganismen; das liegt in der Größenordnung der Zellzahl eines erwachsenen „Standardmenschen“ (30 Billionen)[1]. Die meisten dieser Mikroorganismen leben im Darmtrakt (Darmflora). Daneben ist aber auch die Hautoberfläche (Hautflora) und die Schleimhaut aller Höhlungen des menschlichen Körpers, die mit der Außenwelt direkt oder
indirekt in Verbindung stehen, besiedelt, wie bspw. Mundhöhle, Nasenhöhle, Nasennebenhöhlen, Paukenhöhlen.[2] Sogar im Pankreasgang, der in den Zwölffingerdarm mündet, wurden Pilze nachgewiesen. Auf Schleimhäuten bilden Bakterien häufig Kolonien in Form von Biofilmen.
Gewisse Pilze neigen zur Ausbildung von Geflecht-artigen Strukturen.
Haut und Schleimhäute bilden eine natürliche Barriere, bei deren Verletzung oder Schädigung auch Keime des Mikrobioms in das umgebende Gewebe des menschlichen Körpers oder sogar in die Blutbahn eindringen und Krankheiten auslösen können. Eine ähnliche Gefährdungslage entsteht bei einer Abschwächung des menschlichen Immunsystems durch Medikamente, die standardmäßig nach einer Transplantation zur Verhinderung einer Transplantatabstoßung eingesetzt werden.
Viele Mikroorganismen des Mikrobioms sind nur Kommensalen. Bei anderen hat sich im Verlauf der Evolution durch Langzeitanpassung eine symbiotische Beziehung zu ihrem Wirt, dem Menschen, entwickelt. Voraussetzungen dafür sind komplexe und vielschichtige Beziehungen auf der Ebene von Stoffwechselprozessen, die sich in regulatorischen, intrazellulären und molekulargenetischen Ebenen abbilden.
Dem Darmmikrobiom werden neben der Verwertung der aufgenommenen Nahrung viele weitere wichtige Funktionen zugeschrieben, darunter die Synthese lebenswichtiger Vitamine wie B1, B2, B6, B12 und K, die Produktion kurzkettiger Fettsäuren wie Essigsäure (Acetat-Anion) und Buttersäure (Butyrat-Anion), die als Energiequelle für die Darmschleimhautzellen dienen und das Darmmilieu mitbestimmen, die Förderung der Darmperistaltik über kurzkettige Fettsäuren, die Bekämpfung von Entzündungen, die Entgiftung von Fremdstoffen, die Unterstützung der Verdauung durch den Abbau schwer verdaulicher Nahrungsbestandteile (Ballaststoffe), die Stimulation des Immunsystems, die Verdrängung von Krankheitserregern und mehr. Veränderungen des Darmmikrobioms stehen unter anderem mit Erkrankungen wie Darmentzündungen, Darmtumoren und Darmkrebs, Adipositas, metabolischem Syndrom, Arthritis und auch bestimmte Formen des Autismus und Morbus Alzheimer in Zusammenhang. Tierversuche zeigen, dass ein verändertes, ungünstiges Mikrobiom zu Angstzuständen führen kann bzw. das Ausmaß der Angst beeinflusst und damit maßgeblich auch für die psychische Gesundheit verantwortlich zu sein scheint.
Nicht alle Bakterien in unserem Darm sind erwünscht. Eine ausgeglichene, gesunde Darmflora besteht überwiegend aus nützlichen, sich positiv auf den Körper auswirkenden Bakterien, aber auch stets aus wenigen unerwünschten, negativ auf den Körper wirkenden Bakterien.
Mithilfe der nützlichen Darmbakterien werden u.a. lebenswichtige Enzyme, Vitamine und Aminosäuren produziert und Schadstoffe, die mit der Nahrung aufgenommen werden, neutralisiert. Deshalb schützt eine gesunde und ausgewogene Darmflora effektiv vor dem Eindringen und der Vermehrung von Krankheitserregern. Damit gilt der Darm, der ca. 80% aller Immunantworten des gesamten Organismus reguliert, als Immunorgan Nummer 1.
Auch die neuronale Verbindung von Darm und Gehirn ist zentral für das menschliche Wesen. Die im Darm lebenden Mikroben steuern bspw. die Produktion wichtiger Hormone, darunter das Glückshormon Serotonin und das Schlafhormon Melatonin. So werden über die Darm-Hirn-Achse neurologische Vorgänge im Gehirn gesteuert und die Darmflora beeinflusst maßgeblich die mentale Gesundheit und somit unser Wohlbefinden.
Ein Ungleichgewicht der Darm-Mikrobiota kann durch anhaltende körperliche und seelische Stresssituationen, ungesunde Ernährungsgewohnheiten, unzureichende Bewegung sowie durch Medikamente wie z.B. Antibiotika ausgelöst werden. Hierdurch können verschiedenste Beschwerden auftreten, wie beispielsweise:
Darmbeschwerden (Verstopfung, Blähungen, Bauchschmerzen)
Ausbildung von Auto-Immunreaktionen wie Schuppenflechte (Psoriasis)
Lebensmittelunverträglichkeiten
Übergewicht und Adipositas
Psychischen Störungen
Die Herstellung des Gleichgewichts der Darmflora und damit die Harmonisierung des Mikrobioms kann durch die Einnahme von BranWell unterstützt werden.
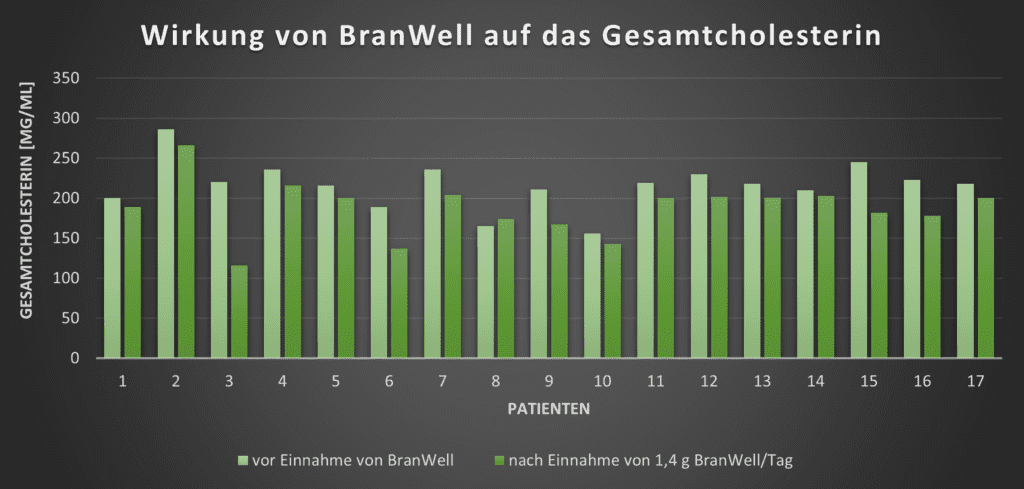
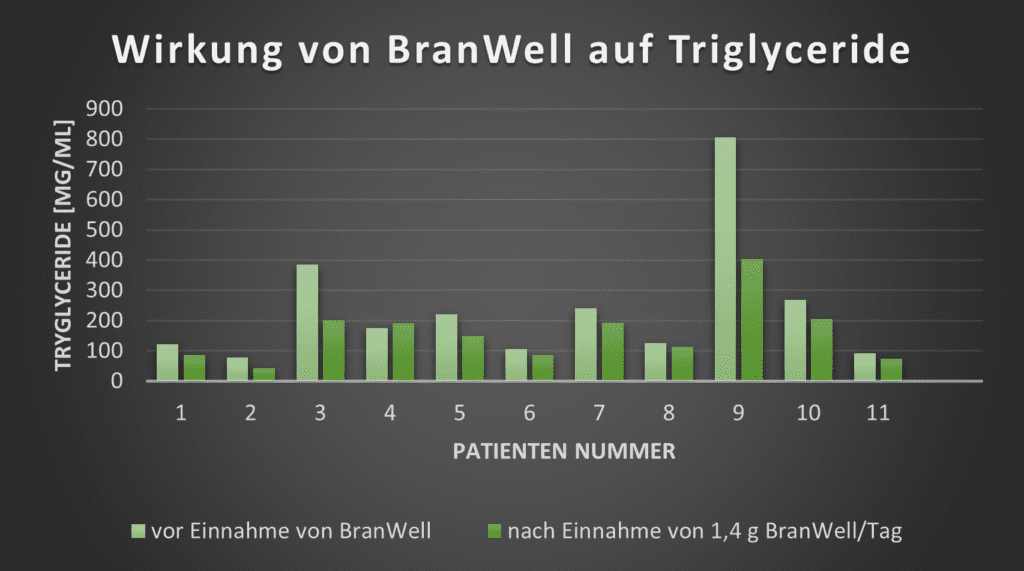
BranWell ist ein reines Naturprodukt aus fermentierter Reiskleie und zeigt neben schnellem Abheilen der für Schuppenflechte typischen Plaques auch eine Reduzierung der Blutfettwerte und Trigylceride.
[1] https://www.biorxiv.org/content/10.1101/036103v1
[2] Werner Bär: Physiologische
Bakterienflora: Kolonisationsresistenz, endogene Opportunisteninfektionen;
Probiotika. In Helmut Hahn, Stefan H. E. Kaufmann, Thomas F. Schulz,
Sebastian Suerbaum: Medizinische Mikrobiologie und Infektiologie.
Springer, Berlin/ Heidelberg/ New York 2009, ISBN 978-3-540-46359-7, S.26 f